登録試験について
1- HOME
- 登録試験について
横スクロールでご覧いただけます
| 臨床試験 | Phase | 試験説明 | 実施期間 | 登録症例数 | 併用化学療法 | 計画照射線量 | 報告年 | |
|---|---|---|---|---|---|---|---|---|
| 初回 | 2回目 | |||||||
| JCOG9812 | III | 高齢者切除不能局所進行型非小細胞肺がんに対する 胸部放射線単独と低用量連日カルボプラチン+胸部放射線同時併用療法とのランダム化比較第III相試験 | 1999/11- 2001/02 |
23 | Daily CBDCA | 60Gy、 2Gy/fr |
20052 | |
| 23 | なし(放射線単独) | |||||||
| JCOG0301 | III | 高齢者切除不能局所進行型非小細胞肺がんに対する 胸部放射線単独と低用量連日カルボプラチン+胸部放射線同時併用療法とのランダム化比較第III相試験 | 2003/09- 2010/03 |
100 | Daily CBDCA | 60Gy、 2Gy/fr |
20123 | 20184 |
| 100 | なし(放射線単独) | |||||||
| NJLCG0601 | II | 切除不能局所進行期非小細胞肺がんに対するシスプラチン+UFT+同時胸部放射線照射とシスプラチン+ビノレルビン+同時胸部放射線照射の無作為化比較第II相試験 | 2006/02- 2009/05 |
35 |
CDDP + UFT |
60Gy、 2Gy/fr |
20135 | |
| 31 |
CDDP + VNB |
|||||||
| OLCSG0007 | III | 局所進行型非小細胞肺がんに対するシスプラチン+ドセタキセル+胸部放射線同時併用とシスプラチン+マイトマイシン+ビンデシン+胸部放射線同時併用とのランダム化比較第III相試験 | 2000/07- 2005/07 |
99 |
CDDP + DTX |
60Gy、 2Gy/fr |
20106 | |
| 101 | CDDP + MMC + VDS |
|||||||
| SPECTRA | II | 局所進行非扁平上皮非小細胞肺癌に対するシスプラチン+S-1同時胸部放射線治療とシスプラチン+ペメトレキセド同時胸部放射線治療の無作為化第II相試験 | 2013/01- 2016/10 |
52 |
CDDP + S-1 |
60Gy、 2Gy/fr |
20207 | |
| 50 |
CDDP + PEM |
|||||||
| TORG1018 | II | 根治照射可能III期非小細胞肺癌に対するシスプラチン+TS-1+TRT併用療法とシスプラチン+ドセタキセル+TRT併用療法のランダム化第II相試験 | 2011/05- 2014/08 |
53 |
CDDP + S-1 |
60Gy、 2Gy/fr |
20208 | |
| 53 |
CDDP + DTX |
|||||||
| WJTOG0105 | III | 切除不能局所進行非小細胞肺癌に対するシスプラチン+S-1とシスプラチン+ビノレルビンと胸部同時放射線照射の無作為化比較第II相試験 | 2001/09- 2005/09 |
153 | CDDP + MMC + VDS |
60Gy、 2Gy/fr |
20109 | 202010 |
| 152 | weekly CBDCA + PTX |
|||||||
| 151 | weekly CBDCA + CPT-11 |
|||||||
| WJOG5008L | II | 切除不能Ⅲ期非小細胞肺癌に対するマイトマイシン+ビンデシン+シスプラチンとイリノテカン+カルボプラチンとパクリタキセル+カルボプラチンと同時放射線治療の無作為化比較第Ⅲ相試験 | 2009/09- 2012/09 |
56 |
CDDP + S-1 |
60Gy、 2Gy/fr |
201811 | |
| 56 |
CDDP + VNB |
|||||||
| 合計 | 1288 | |||||||
JCOG;日本臨床腫瘍研究グループ、
NJLCG;北日本肺癌臨床研究会、OLCSG;岡山肺癌治療研究会、WJOG;西日本がん研究機構、WJTOG;西日本胸部腫瘍臨床研究機構、NSCLC;非小細胞肺癌、CBDCA;
カルボプラチン、CDDP; シスプラチン、UFT;
テガフール/ウラシル、S-1;
テガフール/ギメラシル/オテラシルカリウム、PEM;
ペメトレキセド、DTX; ドセタキセル、MMC; マイトマイシン、VDS;
ビンデシン、PTX; パクリタキセル、CPT-11; イリノテカン、VNR;
ビノレルビン、Gy; グレイ、fr; 分割.
引用各論文はDOIにリンクしています
-
- Ozawa Y, Yamamoto N, et al.
- Creation of an integrated clinical trial database and data sharing for conducting new research by the Japanese Lung Cancer Society.
- JTO Clinical and Research Reports 2022;3:100317.
-
- Atagi S, Kawahara M, Tamura T, et al.
- Standard Thoracic Radiotherapy With or Without Concurrent Daily Low-dose Carboplatin in Elderly Patients with Locally Advanced Non-small Cell Lung Cancer: a Phase III Trial of the Japan Clinical Oncology Group (JCOG9812).
- Japanese Journal of Clinical Oncology 2005;35:195-201.
-
- Atagi S, Kawahara M, Yokoyama A, et al.
- Thoracic radiotherapy with or without daily low-dose carboplatin in elderly patients with non-small-cell lung cancer: a randomised, controlled, phase 3 trial by the Japan Clinical Oncology Group (JCOG0301).
- The Lancet Oncology 2012;13:671-678.
-
- Atagi S, Mizusawa J, Ishikura S, et al.
- Chemoradiotherapy in Elderly Patients With Non-Small-Cell Lung Cancer: Long-Term Follow-Up of a Randomized Trial (JCOG0301).
- Clinical lung cancer 2018;19:e619-e627.
-
- Sugawara S, Maemondo M, Tachihara M, et al.
- Randomized phase II trial of uracil/tegafur and cisplatin versus vinorelbine and cisplatin with concurrent thoracic radiotherapy for locally advanced unresectable stage III non-small-cell lung cancer: NJLCG 0601.
- Lung Cancer 2013;81:91-96.
-
- Segawa Y, Kiura K, Takigawa N, et al.
- Phase III trial comparing docetaxel and cisplatin combination chemotherapy with mitomycin, vindesine, and cisplatin combination chemotherapy with concurrent thoracic radiotherapy in locally advanced non-small-cell lung cancer: OLCSG 0007.
- J Clin Oncol 2010;28:3299-3306.
-
- Yamamoto N, Nakagawa K, Nishimura Y, et al.
- Phase III study comparing second- and third-generation regimens with concurrent thoracic radiotherapy in patients with unresectable stage III non-small-cell lung cancer: West Japan Thoracic Oncology Group WJTOG0105.
- J Clin Oncol 2010;28:3739-3745.
-
- Zenke Y, Tsuboi M, Chiba Y, et al.
- Effect of Second-generation vs Third-generation Chemotherapy Regimens With Thoracic Radiotherapy on Unresectable Stage III Non-Small-Cell Lung Cancer: 10-Year Follow-up of a WJTOG0105 Phase 3 Randomized Clinical Trial.
- JAMA Oncology 2021;7:904-909
-
- Sasaki T, Seto T, Yamanaka T, et al.
- A randomised phase II trial of S-1 plus cisplatin versus vinorelbine plus cisplatin with concurrent thoracic radiotherapy for unresectable, locally advanced non-small cell lung cancer: WJOG5008L.
- Br J Cancer 2018;119:675-682.
-
- Niho S, Yoshida T, Akimoto T, et al.
- Randomized phase II study of chemoradiotherapy with cisplatin + S-1 versus cisplatin + pemetrexed for locally advanced non-squamous non-small cell lung cancer: SPECTRA study.
- Lung Cancer 2020;141:64-71.
-
- Shimokawa T, Yamada K, Tanaka H, et al.
- Randomized phase II trial of S-1 plus cisplatin or docetaxel plus cisplatin with concurrent thoracic radiotherapy for inoperable stage III non-small cell lung cancer.
- Cancer Med 2021;10:626-633.
解析可能項目及び項目別症例数
臨床試験項目の詳細
| 項目 | 中央値(範囲) | ||
|---|---|---|---|
| 年齢;歳 | 66 (30-93) | ||
| 性別 | 男 | 1064 | |
| 女 | 224 | ||
| 病期 | IIIA | 535 | |
| IIIB | 752 | ||
| 体表面積;m2 | 1.622 (1.1-2.35) | ||
| BMI | 21.8 | ||
| 組織型 | 扁平上皮癌 | 517 | |
| 腺癌 | 629 | ||
| その他 | 138 | ||
| 不明 | 3 | ||
| 原発巣の部位 | 右上葉 | 389 | |
| 右中葉 | 19 | ||
| 右下葉 | 121 | ||
| 左上葉 | 276 | ||
| 左下葉 | 78 | ||
| その他 | 33 | ||
| 喫煙期間;年 | 40 (1-70) | ||
| 喫煙量;本 | 20 (1-100) | ||
| TNM分類 | T | 0 | 3 |
| 1 | 172 | ||
| 2 | 391 | ||
| 3 | 177 | ||
| 4 | 476 | ||
| X | 2 | ||
| N | 0 | 72 | |
| 1 | 53 | ||
| 2 | 775 | ||
| 3 | 321 | ||
| PS | 0 | 606 | |
| 1 | 652 | ||
| 2 | 10 | ||
| 総照射線量;Gy | 60(0-70) | ||
| 併用抗がん剤 | CDDP/MMC/VDS | 254 | |
| CDDP/S-1 | 161 | ||
| CDDP/DTX | 152 | ||
| CBDCA/CPT-11 | 152 | ||
| CBDCA/PTX | 151 | ||
| CBDCA (daily) | 123 | ||
| CDDP/VNR | 56 | ||
| CDDP/PEM | 50 | ||
| VNR | 31 | ||
| UFT | 35 | ||
| なし | 123 | ||
| 観察期間;月 | 23.8 (0.3-203) | ||
BMI; body mass index、PS; performance status、Gy;
gray、CDDP; シスプラチン、VDS; ビンデシン、MMC;
マイトマイシン、S-1;
テガフール/ギメラシル/オテラシルカリウム、DTX;ドセタキセル、CBDCA;
カルボプラチン、CPT-11; イリノテカン、PTX;
パクリタキセル、VNR; ビノレルビン、PEM; ペメトレキセド、UFT;
テガフール/ウラシル.
JIDB収載項目及び有効症例数
| 項目 | 有効症例数 | 定義 |
|---|---|---|
| 治療前 全項目 | ||
| 登録日 | 1288 | 日付 |
| 性別 | 1288 | M, F |
| 年齢 | 1288 | 数値 |
| TNM分類:T | 1221 | T0, T1, T2, T3, T4, TX |
| TNM分類:N | 1221 | N0, N1, N2, N3, NX |
| TNM分類:M | 1287 | ⅢA,ⅢB |
| 割付結果 | 1288 | Allocated group |
| 身長(cm) | 822 | 数値 |
| 体重(kg) | 1022 | 数値 |
| 体表面積(㎡) | 822 | 数値 |
| BMI | 822 | 数値 |
| 喫煙歴 | 1021 | Never, Ex, Current |
| Brinkman index | 892 | 数値 |
| 既往/合併有無 | 1021 | 有、無 |
| 既往/合併ー糖尿病 | 1021 | 有、無 |
| 既往/合併ー高血圧 | 1021 | テキストデータ |
| 既往/合併ー不整脈 | 1021 | 有、無 |
| 既往/合併-COPD | 775 | 有、無 |
| 既往/合併-肺気腫 | 775 | 有、無 |
| 既往/合併-気管支喘息 | 775 | 有、無 |
| 既往/合併-その他 | 1021 | 有、無 |
| 既往/合併テキスト | 405 | テキストデータ |
| 6ヶ月以内の体重減少(5kg以上) | 1004 | 有、無 |
| 原発巣の部位-右上葉 | 915 | 有、無 |
| 原発巣の部位-右中葉 | 915 | 有、無 |
| 原発巣の部位-右下葉 | 915 | 有、無 |
| 原発巣の部位-左上葉 | 915 | 有、無 |
| 原発巣の部位-左下葉 | 915 | 有、無 |
| 原発巣の部位-その他 | 915 | 有、無 |
| 原発巣の部位ーその他詳細 | 33 | テキストデータ |
| 組織型 | 1287 | 腺癌、扁平上皮癌、その他のNSCLC,その他、不明 |
| 組織型-その他内容 | 9 | テキストデータ |
| 組織型テキスト | 85 | テキストデータ |
| EGFR変異検査結果 | 274 | 陽性、陰性、不明 |
| EGFR変異詳細 | 36 | テキストデータ |
| 治療前PS | 1268 | 0, 1, 2 |
| 治療前PS確認日 | 108 | 日付 |
| CBC検査日 | 910 | 日付 |
| 白血球数(/mm3) | 911 | 数値 |
| 好中球数(/mm3) | 909 | 数値 |
| ヘモグロビン(g/dL) | 911 | 数値 |
| 血小板数(×10^4/mm3) | 911 | 数値 |
| RBC(×10^4/mm3) | 499 | 数値 |
| 生化学検査日 | 911 | 日付 |
| 総ビリルビン(mg/dL) | 911 | 数値 |
| GOT(AST)(IU/L) | 911 | 数値 |
| GPT(ALT)(IU/L) | 911 | 数値 |
| 血清クレアチニン(mg/dL) | 911 | 数値 |
| TP(g/dL) | 804 | 数値 |
| Blood urea nitrogen(mg/dL) | 805 | 数値 |
| Alb(g/dL) | 908 | 数値 |
| Na(mEq/l) | 910 | 数値 |
| Alkaline phosphatase(IU/l) | 704 | 数値 |
| K(mEq/l) | 910 | 数値 |
| Lactate dehydrogenase(IU/l) | 803 | 数値 |
| Cl(mEq/l) | 603 | 数値 |
| Ca(補正値)(mg/dl) | 897 | 数値 |
| CCR検査日 | 152 | 数値 |
| CCr(補正値)(ml/min) | 152 | 数値 |
| CCr計算方法 | 36 | Cock-croft,蓄尿法 |
| CRP検査日 | 805 | 日付 |
| CRP(mg/dl) | 802 | 数値 |
| 血液ガス検査日 | 801 | 日付 |
| PaO2(torr) | 802 | 数値 |
| PaCO2(torr) | 801 | 数値 |
| KL-6検査日 | 538 | 日付 |
| KL-6 | 533 | 数値 |
| 心電図検査日 | 302 | 日付 |
| 心電図異常 | 344 | 有、無,不明 |
| 心電図異常詳細 | 69 | テキストデータ |
| 試験治療開始後 検査値 | ||
| WBC最低値測定日 | 889 | 日付 |
| WBC grade | 1260 | 0, 1, 2, 3, 4 |
| Hb最低値測定日 | 890 | 日付 |
| Hb grade | 1062 | 0, 1, 2, 3, 4 |
| PLT最低値測定日 | 884 | 日付 |
| PLT grade | 1252 | 0, 1, 2, 3, 4 |
| 好中球最低値測定日 | 889 | 日付 |
| 好中球 grade | 1259 | 0, 1, 2, 3, 4 |
| RBC最低値測定日 | 440 | 日付 |
| RBC 最低値 | 440 | 0, 1, 2, 3, 4 |
| TP最低値測定日 | 776 | 日付 |
| TP 最低値 | 776 | 数値 |
| Alb最低値測定日 | 881 | 日付 |
| Alb grade | 881 | 0, 1, 2, 3, 4 |
| T-Bill最高値測定日 | 866 | 日付 |
| T-Bil grade | 971 | 0, 1, 2, 3, 4 |
| GOT(AST)最高値測定日 | 870 | 日付 |
| GOT grade | 975 | 0, 1, 2, 3, 4 |
| GPT(ALT)最高値測定日 | 870 | 日付 |
| GPT grade | 976 | 0, 1, 2, 3, 4 |
| Lactate dehydrogenase最高値測定日 | 781 | 日付 |
| Lactate dehydrogenase 最高値 | 781 | 数値 |
| Cr最高値測定日 | 868 | 日付 |
| Cr grade | 974 | 0, 1, 2, 3, 4 |
| BUN最高値測定日 | 782 | 日付 |
| BUN最高値 | 782 | 数値 |
| ALP最高値測定日 | 589 | 日付 |
| ALP grade | 589 | 0, 1, 2, 3, 4 |
| Cl最低値測定日 | 588 | 日付 |
| Cl 最低値 | 588 | 数値 |
| Na最高値測定日 | 866 | 日付 |
| Na grade | 866 | 0, 1, 2, 3, 4 |
| Na最低値測定日 | 884 | 日付 |
| Na grade | 884 | 0, 1, 2, 3, 4 |
| K最高値測定日 | 869 | 日付 |
| K grade | 869 | 0, 1, 2, 3, 4 |
| K最低値測定日 | 870 | 日付 |
| K grade | 870 | 0, 1, 2, 3, 4 |
| Ca最高値測定日 | 792 | 日付 |
| Ca grade | 792 | 0, 1, 2, 3, 4 |
| Ca最低値測定日 | 807 | 日付 |
| Ca grade | 807 | 0, 1, 2, 3, 4 |
| SpO2最低値測定日 | 236 | 日付 |
| SpO2 最低値 | 236 | 数値 |
| PaO2最低値測定日 | 508 | 日付 |
| PaO2 最低値 | 509 | 数値 |
| PaCO2最高値測定日 | 400 | 日付 |
| PaCO2 最高値 | 401 | 数値 |
| 試験治療開始から終了まで 臨床所見 | ||
| 治療中 PS最悪値 | 644 | 0, 1, 2, 3, 4 |
| 治療中 PS最悪値確認週(治療開始より) | 532 | 数値 |
| 治療中 呼吸困難(息切れ) 最悪Grade | 886 | 0, 1, 2, 3, 4, 5 |
| 治療中 呼吸困難(息切れ)最悪Grade確認週(治療開始より) | 690 | 数値 |
| 治療中 肺臓炎/肺浸潤 最悪Grade | 977 | 0, 1, 2, 3, 4, 5 |
| 治療中 肺臓炎/肺浸潤 最悪Grade確認週(治療開始より) | 685 | 数値 |
| 治療中 左心室機能 最悪Grade | 45 | 0, 1, 2, 3, 4, 5 |
| 治療中 左心室機能 最悪Grade確認週(治療開始より) | 45 | |
| 治療中 心嚢水/心嚢炎 最悪Grade | 341 | 数値 |
| 治療中 心嚢水/心嚢炎 最悪Grade確認週(治療開始より) | 239 | |
| 治療中 浮腫 最悪Grade | 347 | 0, 1, 2, 3, 4, 5 |
| 治療中 浮腫 最悪Grade確認週(治療開始より) | 241 | 数値 |
| 治療中 疲労(嗜眠、倦怠感、無力) 最悪Grade | 902 | 0, 1, 2, 3, 4, 5 |
| 治療中 疲労(嗜眠、倦怠感、無力) 最悪Grade確認週(治療開始より) | 769 | 数値 |
| 治療中 発熱 最悪Grade | 982 | 0, 1, 2, 3, 4, 5 |
| 治療中 発熱 最悪Grade確認週(治療開始より) | 725 | 数値 |
| 治療中 放射線皮膚炎 最悪Grade | 905 | 0, 1, 2, 3, 4, 5 |
| 治療中 放射線皮膚炎 最悪Grade確認週(治療開始より) | 832 | 数値 |
| 治療中 食欲不振 最悪Grade | 502 | 0, 1, 2, 3, 4, 5 |
| 治療中 食欲不振 最悪Grade確認週(治療開始より) | 348 | 数値 |
| 治療中 放射線による食道嚥下困難 最悪Grade | 786 | 0, 1, 2, 3, 4, 5 |
| 治療中 放射線による食道嚥下困難 最悪Grade確認週(治療開始より) | 739 | 数値 |
| 治療中 悪心 最悪Grade | 989 | 0, 1, 2, 3, 4, 5 |
| 治療中 悪心 最悪Grade確認週(治療開始より) | 815 | 数値 |
| 治療中 嘔吐 最悪Grade | 986 | 0, 1, 2, 3, 4, 5 |
| 治療中 嘔吐 最悪Grade確認週(治療開始より) | 711 | 数値 |
| 治療中 発熱性好中球減少 最悪Grade | 988 | 0, 1, 2, 3, 4, 5 |
| 治療中 発熱性好中球減少 最悪Grade確認週(治療開始より) | 693 | 数値 |
| 治療中 咳 最悪Grade | 343 | 0, 1, 2, 3, 4, 5 |
| 治療中 咳 最悪Grade確認週(治療開始より) | 245 | 数値 |
| 治療中 下痢 最悪Grade | 747 | 0, 1, 2, 3, 4, 5 |
| 治療中 下痢 最悪Grade確認週(治療開始より) | 477 | 数値 |
| 治療中 便秘 最悪Grade | 752 | 0, 1, 2, 3, 4, 5 |
| 治療中 便秘 最悪Grade確認週(治療開始より) | 593 | 数値 |
| 治療中 感染 最悪Grade | 841 | 0, 1, 2, 3, 4, 5 |
| 治療中 感染 最悪Grade確認週(治療開始より) | 654 | 数値 |
| 治療中 口内炎/咽頭炎(口腔/咽頭粘膜炎) 最悪Grade | 750 | 0, 1, 2, 3, 4, 5 |
| 治療中 口内炎/咽頭炎(口腔/咽頭粘膜炎) 最悪Grade確認週(治療開始より) | 474 | 数値 |
| 治療中 神経障害(運動性) 最悪Grade | 752 | 0, 1, 2, 3, 4, 5 |
| 治療中 神経障害(運動性) 最悪Grade確認週(治療開始より) | 445 | 数値 |
| 治療中 神経障害(感覚性) 最悪Grade | 749 | 0, 1, 2, 3, 4, 5 |
| 治療中 神経障害(感覚性) 最悪Grade確認週(治療開始より) | 455 | 数値 |
| 治療中 食道炎 最悪Grade | 255 | 0, 1, 2, 3, 4, 5 |
| 治療中 食道炎 最悪Grade確認週(治療開始より) | 165 | 数値 |
| 治療中 脱毛 最悪Grade | 305 | 0, 1, 2, 3, 4, 5 |
| 治療中 脱毛 最悪Grade確認週(治療開始より) | 19 | 数値 |
| 治療中 アレルギー反応 最悪Grade | 208 | 0, 1, 2, 3, 4, 5 |
| 治療中 アレルギー反応 最悪Grade確認週(治療開始より) | 1 | 数値 |
| 治療中 肺線維症 最悪Grade | 208 | 0, 1, 2, 3, 4, 5 |
| 治療中 肺線維症 最悪Grade確認週(治療開始より) | 0 | 数値 |
| 試験治療終了から最終観察日まで 臨床所見 | 0, 1, 2, 3, 4, 5 | |
| 治療後 PS最悪値 | 607 | 数値 |
| 治療後 PS最悪値確認週(治療開始より) | 74 | 数値 |
| 治療後 呼吸困難 最悪Grade | 838 | 0, 1, 2, 3, 4 |
| 治療後 呼吸困難 最悪Grade確認週(治療開始より) | 210 | 数値 |
| 治療後 肺臓炎/肺浸潤 最悪Grade | 972 | 0, 1, 2, 3, 4, 5 |
| 治療後 肺臓炎/肺浸潤 最悪Grade確認週(治療開始より) | 328 | 数値 |
| 治療後 左心室機能 最悪Grade | 0 | 0, 1, 2, 3, 4, 5 |
| 治療後 左心室機能 最悪Grade確認週(治療開始より) | 0 | 数値 |
| 治療後 心嚢水/心嚢炎 最悪Grade | 612 | 0, 1, 2, 3, 4, 5 |
| 治療後 心嚢水/心嚢炎 最悪Grade確認週(治療開始より) | 239 | 数値 |
| 治療後 浮腫 最悪Grade | 285 | 0, 1, 2, 3, 4, 5 |
| 治療後 浮腫 最悪Grade確認週(治療開始より) | 194 | 数値 |
| 治療後 疲労(嗜眠、倦怠感、無力) 最悪Grade | 819 | 0, 1, 2, 3, 4, 5 |
| 治療後 疲労(嗜眠、倦怠感、無力) 最悪Grade確認週(治療開始より) | 264 | 数値 |
| 治療後 発熱 最悪Grade | 887 | 0, 1, 2, 3, 4, 5 |
| 治療後 発熱 最悪Grade確認週(治療開始より) | 222 | 数値 |
| 治療後 放射線皮膚炎 最悪Grade | 836 | 0, 1, 2, 3, 4, 5 |
| 治療後 放射線皮膚炎 最悪Grade確認週(治療開始より) | 281 | 数値 |
| 治療後 食欲不振 最悪Grade | 452 | 0, 1, 2, 3, 4, 5 |
| 治療後 食欲不振 最悪Grade確認週(治療開始より) | 291 | 数値 |
| 治療後 放射線による食道嚥下困難 最悪Grade | 698 | 0, 1, 2, 3, 4, 5 |
| 治療後 放射線による食道嚥下困難 最悪Grade確認週(治療開始より) | 219 | 数値 |
| 治療後 悪心 最悪Grade | 893 | 0, 1, 2, 3, 4, 5 |
| 治療後 悪心 最悪Grade確認週(治療開始より) | 285 | 数値 |
| 治療後 嘔吐 最悪Grade | 906 | 0, 1, 2, 3, 4, 5 |
| 治療後 嘔吐 最悪Grade確認週(治療開始より) | 219 | 数値 |
| 治療後 発熱性好中球減少 最悪Grade | 909 | 0, 1, 2, 3, 4, 5 |
| 治療後 発熱性好中球減少 最悪Grade確認週(治療開始より) | 210 | 数値 |
| 治療後 咳 最悪Grade | 300 | 0, 1, 2, 3, 4, 5 |
| 治療後 咳 最悪Grade確認週(治療開始より) | 204 | 数値 |
| 治療後 下痢 最悪Grade | 702 | 0, 1, 2, 3, 4, 5 |
| 治療後 下痢 最悪Grade確認週(治療開始より) | 20 | 数値 |
| 治療後 便秘 最悪Grade | 683 | 0, 1, 2, 3, 4, 5 |
| 治療後 便秘 最悪Grade確認週(治療開始より) | 79 | 数値 |
| 治療後 感染 最悪Grade | 826 | 0, 1, 2, 3, 4, 5 |
| 治療後 感染 最悪Grade確認週(治療開始より) | 219 | 数値 |
| 治療後 口内炎/咽頭炎(口腔/咽頭粘膜炎) 最悪Grade | 710 | 0, 1, 2, 3, 4, 5 |
| 治療後 口内炎/咽頭炎(口腔/咽頭粘膜炎) 最悪Grade確認週(治療開始より) | 21 | 数値 |
| 治療後 神経障害(運動性) 最悪Grade | 721 | 0, 1, 2, 3, 4, 5 |
| 治療後 神経障害(運動性) 最悪Grade確認週(治療開始より) | 8 | 数値 |
| 治療後 神経障害(感覚性) 最悪Grade | 714 | 0, 1, 2, 3, 4, 5 |
| 治療後 神経障害(感覚性) 最悪Grade確認週(治療開始より) | 17 | 数値 |
| 治療後 食道炎 最悪Grade | 485 | 0, 1, 2, 3, 4, 5 |
| 治療後 食道炎 最悪Grade確認週(治療開始より) | 92 | 数値 |
| 治療後 脱毛 最悪Grade | 281 | 0, 1, 2, 3, 4, 5 |
| 治療後 脱毛 最悪Grade確認週(治療開始より) | 27 | 数値 |
| 治療後 アレルギー反応 最悪Grade | 177 | 0, 1, 2, 3, 4, 5 |
| 治療後 アレルギー反応 最悪Grade確認週(治療開始より) | 0 | 数値 |
| 治療後 肺線維症 最悪Grade | 192 | 0, 1, 2, 3, 4, 5 |
| 治療後 肺線維症 最悪Grade確認週(治療開始より) | 4 | 数値 |
| 全経過 臨床所見 | ||
| 全経過 PS最悪値 | 650 | 0, 1, 2, 3, 4, 5 |
| 全経過 PS最悪値確認週(治療開始より) | 468 | 数値 |
| 全経過 呼吸困難 最悪Grade | 892 | |
| 全経過 呼吸困難 最悪Grade確認週(治療開始より) | 652 | 0, 1, 2, 3, 4 |
| 全経過 肺臓炎/肺浸潤 最悪Grade | 1203 | 数値 |
| 全経過 肺臓炎/肺浸潤最悪Grade確認週(治療開始より) | 565 | 0, 1, 2, 3, 4, 5 |
| 全経過 左心室機能 最悪Grade | 45 | 数値 |
| 全経過 左心室機能 最悪Grade確認週(治療開始より) | 45 | 0, 1, 2, 3, 4, 5 |
| 全経過 心嚢水/心嚢炎 最悪Grade | 615 | 数値 |
| 全経過 心嚢水/心嚢炎 最悪Grade確認週(治療開始より) | 241 | 0, 1, 2, 3, 4, 5 |
| 全経過 浮腫 最悪Grade | 347 | |
| 全経過 浮腫 最悪Grade確認週(治療開始より) | 241 | 0, 1, 2, 3, 4, 5 |
| 全経過 疲労(嗜眠、倦怠感、無力) 最悪Grade | 927 | 数値 |
| 全経過 疲労(嗜眠、倦怠感、無力) 最悪Grade確認週(治療開始より) | 713 | 0, 1, 2, 3, 4, 5 |
| 全経過 発熱 最悪Grade | 995 | 数値 |
| 全経過 発熱 最悪Grade確認週(治療開始より) | 704 | 0, 1, 2, 3, 4, 5 |
| 全経過 放射線皮膚炎 最悪Grade | 912 | 数値 |
| 全経過 放射線皮膚炎 最悪Grade確認週(治療開始より) | 812 | 0, 1, 2, 3, 4, 5 |
| 全経過 食欲不振 最悪Grade | 576 | 数値 |
| 全経過 食欲不振 最悪Grade確認週(治療開始より) | 361 | 0, 1, 2, 3, 4, 5 |
| 全経過 放射線による食道嚥下困難 最悪Grade | 794 | 数値 |
| 全経過 放射線による食道嚥下困難 最悪Grade確認週(治療開始より) | 726 | 0, 1, 2, 3, 4, 5 |
| 全経過 悪心 最悪Grade | 995 | 数値 |
| 全経過 悪心 最悪Grade確認週(治療開始より) | 773 | 0, 1, 2, 3, 4, 5 |
| 全経過 嘔吐 最悪Grade | 1061 | 数値 |
| 全経過 嘔吐 最悪Grade確認週(治療開始より) | 697 | 0, 1, 2, 3, 4, 5 |
| 全経過 発熱性好中球減少 最悪Grade | 1061 | 数値 |
| 全経過 発熱性好中球減少 最悪Grade確認週(治療開始より) | 681 | 0, 1, 2, 3, 4, 5 |
| 全経過 咳 最悪Grade | 347 | 数値 |
| 全経過 咳 最悪Grade確認週(治療開始より) | 254 | 0, 1, 2, 3, 4, 5 |
| 全経過 下痢 最悪Grade | 822 | 数値 |
| 全経過 下痢 最悪Grade確認週(治療開始より) | 449 | 0, 1, 2, 3, 4, 5 |
| 全経過 便秘 最悪Grade | 756 | 数値 |
| 全経過 便秘 最悪Grade確認週(治療開始より) | 560 | 0, 1, 2, 3, 4, 5 |
| 全経過 感染 最悪Grade | 921 | 数値 |
| 全経過 感染 最悪Grade確認週(治療開始より) | 633 | 0, 1, 2, 3, 4, 5 |
| 全経過 口内炎/咽頭炎(口腔/咽頭粘膜炎) 最悪Grade | 822 | 数値 |
| 全経過 口内炎/咽頭炎(口腔/咽頭粘膜炎) 最悪Grade確認週(治療開始より) | 458 | 0, 1, 2, 3, 4, 5 |
| 全経過 神経障害(運動性) 最悪Grade | 756 | 数値 |
| 全経過 神経障害(運動性) 最悪Grade確認週(治療開始より) | 426 | 0, 1, 2, 3, 4, 5 |
| 全経過 神経障害(感覚性) 最悪Grade | 822 | 数値 |
| 全経過 神経障害(感覚性) 最悪Grade確認週(治療開始より) | 382 | 0, 1, 2, 3, 4, 5 |
| 全経過 食道炎 最悪Grade | 769 | 数値 |
| 全経過 食道炎 最悪Grade確認週(治療開始より) | 213 | 0, 1, 2, 3, 4, 5 |
| 全経過 脱毛 最悪Grade | 381 | 数値 |
| 全経過 脱毛 最悪Grade確認週(治療開始より) | 32 | 0, 1, 2, 3, 4, 5 |
| 全経過 アレルギー反応 最悪Grade | 208 | 数値 |
| 全経過 アレルギー反応 最悪Grade確認週(治療開始より) | 1 | 0, 1, 2, 3, 4, 5 |
| 全経過 肺線維症 最悪Grade | 208 | 数値 |
| 全経過 肺線維症 最悪Grade確認週(治療開始より) | 4 | 0, 1, 2, 3, 4, 5 |
| 臨床試験で規定された放射線治療に関して | ||
| 放射線治療開始日 | 1061 | 日付 |
| 放射線治療終了日 | 993 | 日付 |
| 放射線1回線量(Gy) | 239 | 数値 |
| 回数(回) | 239 | 数値 |
| 総照射線量(Gy) | 1259 | 数値 |
| 照射中止の有無 | 208 | 有、無 |
| 照射中の休止の有無 | 995 | 有、無 |
| 計画外の照射休止日数 | 648 | 数値 |
| 計画外の照射休止理由(血液毒性)-血液毒性の有無 | 319 | 有、無 |
| 計画外の照射休止理由(血液毒性)-WBC:G4 | 276 | 有、無 |
| 計画外の照射休止理由(血液毒性)-ANC:G4 | 276 | 有、無 |
| 計画外の照射休止理由(血液毒性)-PLT:G4 | 276 | 有、無 |
| 計画外の照射休止理由(非血液毒性)-非血液毒性の有無 | 335 | 有、無 |
| 計画外の照射休止理由(非血液毒性)-発熱≧G1 | 319 | 有、無 |
| 計画外の照射休止理由(非血液毒性)-G3食道炎 | 305 | 有、無 |
| 計画外の照射休止理由(非血液毒性)-G3皮膚炎 | 303 | 有、無 |
| 計画外の照射休止理由-G-CSF中 | 276 | 有、無 |
| 計画外の照射休止理由(非血液毒性)-肺臓炎 | 319 | 有、無 |
| 計画外の照射休止理由(その他の有害事象) | 59 | 有、無 |
| 計画外の照射休止理由(その他-有害事象以外) | 82 | 有、無 |
| 計画外の照射休止理由(その他-詳細) | 135 | テキストデータ |
| V20(%) | 209 | 数値 |
| 予定照射門数 | 107 | 数値 |
| 放射線治療完遂状況 | 208 | 有、無 |
| 臨床試験で規定された化学療法に関して | ||
| 化学療法治療開始日 | 502 | 日付 |
| 化学療法治療終了日 | 769 | 日付 |
| 投与中止有無 | 548 | 有、無 |
| 投与中止理由ー血液毒性 | 245 | 有、無 |
| 投与中止理由ー非血液毒性 | 245 | 有、無 |
| 投与中止理由ーその他 | 233 | 有、無 |
| 投与休止の有無 | 353 | 有、無 |
| 投与休止日数 | 58 | 数値 |
| 投与休止理由-血液毒性 | 50 | 有、無 |
| 投与休止理由-非血液毒性 | 50 | 有、無 |
| 投与休止理由-その他 | 50 | 有、無 |
| 投与減量の有無 | 756 | 有、無 |
| 投与減量理由-毒性 | 343 | 有、無 |
| 投与減量理由-その他 | 343 | 有、無 |
| 投与延期の有無 | 661 | 有、無 |
| 投与延期理由-毒性 | 337 | 有、無 |
| 投与延期理由-その他 | 337 | 有、無 |
| 予定された化学療法の完遂 | 102 | 有、無 |
| 腫瘍評価 | ||
| 標的病変 治療前長径和(mm) | 639 | 数値 |
| 標的病変 治療前長径和 検査日 | 637 | 日付 |
| 標的病変 最小長径和 | 627 | 数値 |
| 標的病変縮小割合(%) | 627 | 数値 |
| 標的病変最縮小検査日 | 625 | 日付 |
| 標的病変増大割合(%) | 633 | 数値 |
| 標的病変最増大検査日 | 11 | 日付 |
| 治療期間中の新病変の有無 | 704 | 有、無 |
| 新病変部位-縦隔リンパ節(鎖骨上窩含む) | 129 | 有、無 |
| 新病変部位-胸腔内病変(胸膜・心膜病変を除く) | 129 | 有、無 |
| 新病変部位-胸膜・心膜病変 | 129 | 有、無 |
| 新病変部位-脳病変 | 156 | 有、無 |
| 新病変部位-その他 | 129 | 有、無 |
| 新病変部位テキスト | 129 | テキストデータ |
| 新病変確認日 | 129 | 日付 |
| 新病変診断方法 | 12 | テキストデータ |
| 治療全体における効果 標的病変 | 531 | CR, PR, SD, PD, NE |
| 治療全体における効果 非標的病変 | 293 | CR, non-CR/non-PD, PD, NE |
| 治療全体における効果 新病変の有無 | 524 | 有、無 |
| 治療全体における最良総合効果 | 1249 | CR, PR, SD, PD, NE |
| 治療完遂及び治療効果 | ||
| プロトコール規定の治療完了 | 1073 | 有、無 |
| プロトコール治療に中止 | 1073 | 有、無 |
| 中止判断日 | 379 | 日付 |
| 原病の増悪(PD)のため中止 | 371 | 有、無 |
| 有害事象による中止の有無 | 371 | 有、無 |
| 肺臓炎/肺浸潤による中止 | 336 | 有、無 |
| 肺感染症・感染性肺炎による中止 | 336 | 有、無 |
| PS低下による中止 | 348 | 有、無 |
| 食道炎による中止 | 336 | 有、無 |
| 肺以外の感染症による中止 | 336 | 有、無 |
| 血液毒性による中止 | 336 | 有、無 |
| その他の有害事象による中止 | 336 | 有、無 |
| 有害事象による中止テキスト | 211 | テキストデータ |
| 有害事象に伴う患者拒否により中止 | 370 | 有、無 |
| 有害事象と関連のない患者拒否により中止 | 370 | 有、無 |
| 死亡による中止(プロトコール期間中の死亡) | 370 | 有、無 |
| 中止理由(その他) | 370 | 有、無 |
| 転帰 | 1287 | alive, death, unknown |
| 最終生存確認日 | 557 | 日付 |
| 死亡日 | 943 | 日付 |
| 死因 | 760 | 原疾患による死亡、他疾患による死亡、治療に関連した死亡、その他、不明 |
| 死亡/不明の詳細 | 407 | テキストデータ |
| 放射線治療終了までの 増悪の有無 | 994 | 有、無 |
| 放射線治療終了時までの 増悪・無増悪確認日(増悪または無増悪を確認した最終日) | 985 | 日付 |
| 放射線治療終了時までの 無増悪症例の最終無増悪確認日 | 948 | 日付 |
| 放射線治療終了日以降 増悪の有無 | 994 | 有、無 |
| 放射線治療終了日以降 増悪・無増悪確認日(増悪または無増悪を確認した最終日) | 950 | 日付 |
| 放射線治療終了日以降 無増悪症例の最終無増悪確認日 | 195 | 日付 |
| 全経過 増悪の有無 | 1286 | 有、無 |
| 全経過 増悪・無増悪確認日(増悪または無増悪を確認した最終日) | 1276 | 日付 |
| 全経過 無増悪症例の最終無増悪確認日 | 262 | 日付 |
| 増悪部位-照射野内 | 802 | 有、無 |
| 増悪部位-照射野外 | 802 | 有、無 |
| 増悪部位-照射野その他 | 177 | 有、無 |
| 増悪部位-原発巣 | 571 | 有、無 |
| 増悪部位-リンパ節【すべて】 | 553 | 有、無 |
| 増悪部位-リンパ節【肺門、縦隔、鎖骨】 | 480 | 有、無 |
| 増悪部位-リンパ節【その他】 | 485 | 有、無 |
| 増悪部位-中枢神経病変 | 575 | 有、無 |
| 増悪部位-骨 | 561 | 有、無 |
| 増悪部位-肝臓 | 559 | 有、無 |
| 増悪部位-副腎 | 556 | 有、無 |
| 増悪部位-肺内転移 | 527 | 有、無 |
| 増悪部位-胸水/胸膜炎 | 535 | 有、無 |
| 増悪部位-その他 | 534 | 有、無 |
| 増悪部位テキスト | 583 | テキストデータ |
| 後治療有無 | ||
| 後治療の有無 | 1035 | 有、無 |
| 後治療としての化学療法の有無 | 1042 | 有、無,不明 |
| 化学療法ー①開始日 | 317 | 日付 |
| 化学療法ー①レジメン薬1 | 547 | テキストデータ |
| 化学療法ー①レジメン薬2 | 204 | テキストデータ |
| 化学療法ー①レジメン薬3 | 7 | テキストデータ |
| 化学療法ー①レジメン詳細 | 549 | テキストデータ |
| 化学療法ー②開始日 | 174 | 日付 |
| 化学療法ー②レジメン薬1 | 299 | テキストデータ |
| 化学療法ー②レジメン薬2 | 70 | テキストデータ |
| 化学療法ー②レジメン薬3 | 8 | テキストデータ |
| 化学療法ー②レジメン詳細 | 299 | テキストデータ |
| 化学療法ー③開始日 | 74 | 日付 |
| 化学療法ー③レジメン薬1 | 138 | テキストデータ |
| 化学療法ー③レジメン薬2 | 33 | テキストデータ |
| 化学療法ー③レジメン薬3 | 2 | テキストデータ |
| 化学療法ー③レジメン詳細 | 138 | テキストデータ |
| 後治療としての放射線療法有無 | 843 | 有、無, unknown |
| 放射線療法ー①開始日 | 164 | 日付 |
| 放射線療法-①照射部位 | 30 | テキストデータ |
| 放射線療法ー①照射部位詳細 | 166 | テキストデータ |
| 放射線療法ー①照射量 | 34 | 数値 |
| 放射線療法ー①総照射量 | 49 | 数値 |
| 放射線療法ー②開始日 | 48 | 日付 |
| 放射線療法-②照射部位 | 15 | テキストデータ |
| 放射線療法ー②照射部位詳細 | 50 | テキストデータ |
| 放射線療法ー②照射量 | 13 | 数値 |
| 放射線療法ー②総照射量 | 18 | 数値 |
| 後治療としての切開術有無 | 843 | 有、無,不明 |
| 切開術-手術日 | 48 | 日付 |
| 切開術-手術詳細 | 47 | テキストデータ |
COPD; 慢性閉塞性肺疾患、NSCLC;非小細胞肺癌、EGFR;上皮成長因子受容体、CTCAE;
Common Terminology Criteria for Adverse Events、Gy;
グレイ、CR;完全寛解、PR;部分寛解、SD;病勢安定、PD;腫瘍増悪、NE;評価不可
*Gradeは各臨床試験での判定に基づく
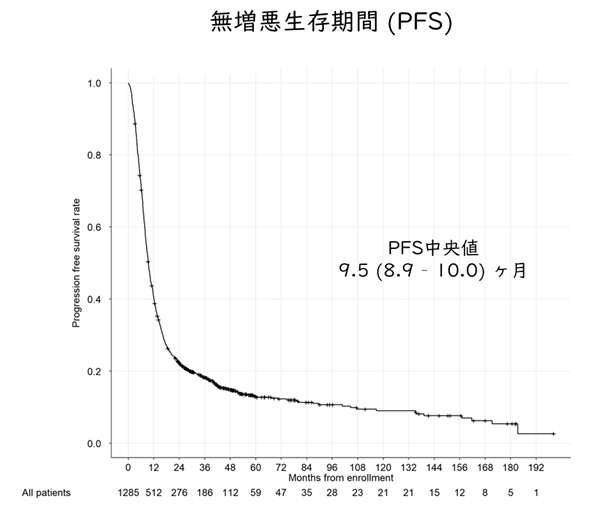
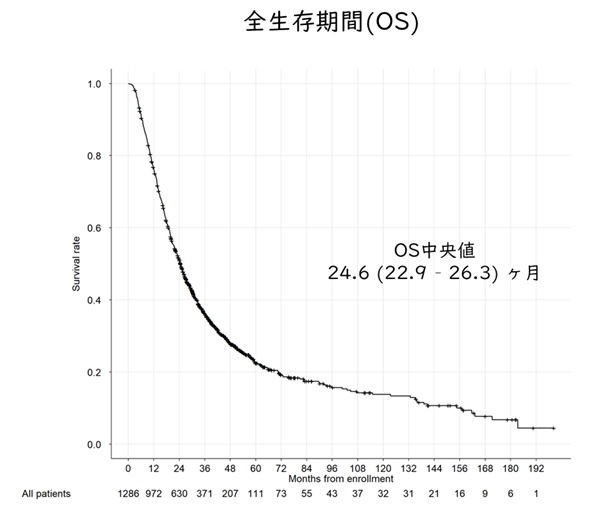
JIDB登録全例における無増悪生存曲線及び生存期間